有源醫療器械加速老化試驗效期驗證及使用期限驗證流程
為了確保醫療器械在生命周期內的安全及有效性,注冊人應在設計開發中對其使用期限予以驗證。使用期限的驗證是醫療器械可靠性研究的重要組成部分,制定并驗證合理的使用期限有
來源:醫療器械注冊代辦 發布日期:2023-10-10 閱讀量:次
?

4月27日,武漢律動醫療科技有限公司的一次性使用胸腔穿刺針,在通過技術審評后,僅用半個小時就完成了醫療器械注冊行政審批環節的審核、核準、審定,獲得了由湖北省藥監局頒發的第二類醫療器械產品注冊證,該產品委托英特姆(武漢)醫療科技有限公司生產。至此,武漢律動醫療科技有限公司的“一次性使用胸腔穿刺針”成為2019年12月4日發布的《關于實施醫療器械注冊人制度試點工作的通告》(湖北省藥品監督管理局通告2019年第11號)后,湖北省首個按照醫療器械注冊人制度試點方案獲批的產品。

注冊人制度試點是服務于改革,充分釋放改革創新紅利的重要舉措,此項審評審批制度的改革,有利于提升湖北省醫療器械產業發展水平;有利于科研人才、研發機構、和創新企業集聚和發展;有利于整合社會資源,推動醫療器械產業鏈分工與合作。
信息來源:湖北省藥監局注冊管理處

站點聲明
本網站所提供的信息僅供參考之用,并不代表本網贊同其觀點,也不代表本網對其真實性負責。圖片版權歸原作者所有,如有侵權請聯系我們,我們立刻刪除。如有關于作品內容、版權或其它問題請于作品發表后的30日內與本站聯系,本網將迅速給您回應并做相關處理。
鄭州思途醫療科技有限公司專注于醫療器械產品政策與法規規事務服務,提供產品注冊備案申報代理、臨床試驗、體系建立輔導、分類界定、申請創新辦理服務。
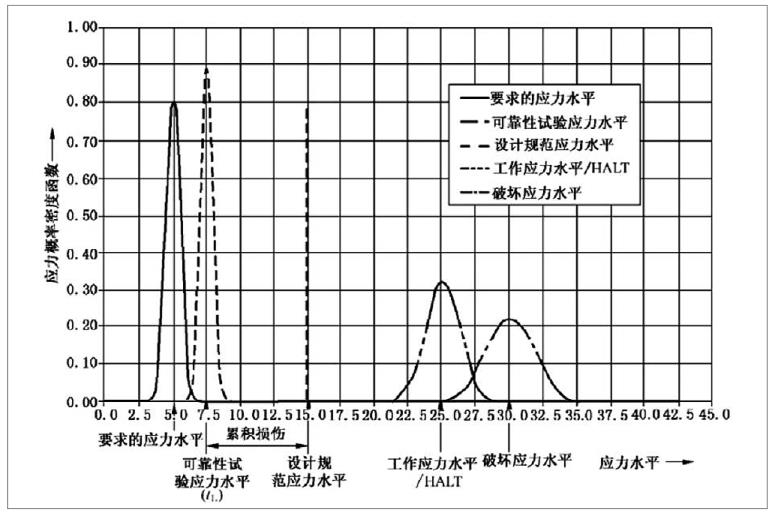
為了確保醫療器械在生命周期內的安全及有效性,注冊人應在設計開發中對其使用期限予以驗證。使用期限的驗證是醫療器械可靠性研究的重要組成部分,制定并驗證合理的使用期限有

國家市場監管總局于官網公布《藥品注冊管理辦法》(以下簡稱“辦法”)已于2020年7月1日起正式施行。國家藥監局從《辦法》修訂的背景、思路、引入了哪些新理念和制度、有哪些鼓

2020年6月29日,國務院發布《化妝品監督管理條例》(國令第727號),規定化妝品新原料需向國務院藥品監督管理部門申請注冊或者備案后才能用于化妝品中。

隨著國家醫療改革的不斷深入,使得綜合性大中型醫療機構的中心實驗室對自動化系統有了新的要求,為了簡化檢測流程,提高檢測效率,保證數據準確度等,中心實驗室對集中化診斷
中國是世界上最有潛力的醫療器械市場及最大市場之一,許多醫療器械進出口貿易商或國外有實力的企業希望能夠按照中國藥監局醫療器械注冊監管要求獲得中國市場的上市準入。考慮

FDA于2020.12.11發布了關于簡短(Abbreviated) 510(k)申請的相關產品指南,該指南是在遵守“基于安全有效性途徑”這一前提下編制提出的。在這個框架下,申請人若計劃使用安全有效性途徑提交

醫療器械注冊費是行政性收費,按照注冊單元收取,部分省份不收取醫療器械注冊費用,絕大部分省份還是收取的。本篇文章統計了截止到2022年1月5日各地醫療器械注冊收費標準。

中國能排進世界十大醫療器械制造強國嗎?暫時還不能,因為排進前十的國家都有許多知名械企和世界級醫療器械巨頭;而中國比較出名的可能只有邁瑞了,其他械企仍需努力了。下面

2020年3月17日國家藥監局發布了關于醫療器械主文檔登記事項的公告(2021年第36號),之前給大家介紹過醫療器械主文檔的主要內容、適用的產品注冊類型等信息。今天我們再來向大家介

本文介紹了歐盟醫療器械新法規MDR相比于將替代的MDD法規的幾點新增要求。建議收藏學習。明年5月份起,Medical Devices Regulation(MDR)(2017/745/ EU)將替代原本的Medical Devices Directive (93
行業資訊
知識分享
八年
醫療器械服務經驗
聯系思途,免費獲得專屬《落地解決方案》及報價
咨詢相關問題或咨詢報價,可以直接與我們聯系
思途CRO——醫療器械注冊臨床第三方平臺
