長江三角洲區域醫療器械注冊人制度試點工作實施方案(試行)(滬藥監械管〔2019〕112號)
為深入貫徹落實中共中央辦公廳、國務院辦公廳印發的《關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》(廳字〔2017〕42號),按照國家藥品監督管理局《關于擴大醫療器械
來源:醫療器械注冊代辦 發布日期:2016-04-27 閱讀量:次
附件:可吸收性外科縫線注冊技術審查指導原則(2016年第70號).doc
本指導原則旨在指導注冊申請人對可吸收性外科縫線產品注冊申報資料的準備及撰寫,同時也為技術審評部門審評注冊申報資料提供參考。
本指導原則是對可吸收性外科縫線產品注冊申報資料的一般要求,申請人應依據具體產品特性確定其中內容是否適用,若不適用,需具體闡述理由及相應的科學依據,并依據產品具體特性對注冊申報資料的內容進行充實和細化。
本指導原則是對申請人和審查人員的指導性文件,不涉及注冊審批等行政事項,亦不作為法規強制執行, 如有能滿足相關法規要求的其他方法,也可以采用,但應提供詳細的研究資料和驗證資料。應當在遵循相關法規的前提下使用本指導原則。
本指導原則是在現行法規和標準體系以及當前認知水平下制定的,隨著法規、標準體系的不斷完善和科學技術的不斷發展,本指導原則相關內容也將適時進行調整。
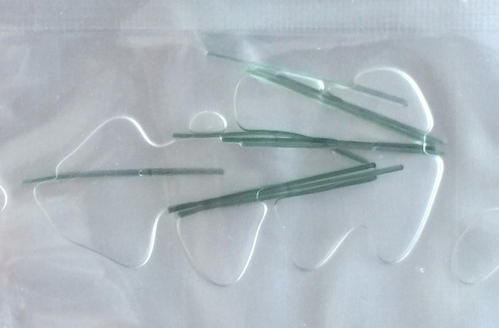
本指導原則所涉及的可吸收性外科縫線(以下簡稱可吸收縫線)是由健康哺乳動物的膠原或人工合成的聚合物加工而成,可被活體哺乳動物組織吸收。涵蓋的材料包括聚乙醇酸(PGA)、乙交酯-丙交酯共聚物(PGLA)、聚對二氧環己酮(PDS)等可吸收合成材料和動物源性材料。可吸收縫線可用合適的涂層、軟化劑浸漬或處理,可以是單股或多股形式。
本指導原則不適用于非吸收性外科縫線。
(一)綜述資料
1.概述
描述申報產品的管理類別、分類編碼及名稱的確定依據。
2.產品描述
產品描述應全面、詳細,至少應包括申報產品名稱、產品組成成分(包括主要材料、涂層和添加劑)和各成分百分比、結構(單股/多股)、制式(平制/鉻制)、染色情況、適用部位、預期用途、技術性能指標及其制定依據、體內吸收及降解特性、降解產物,以及產品的其他詳細特征等內容。必要時提供圖示說明。
3.規格型號
說明產品的規格型號及劃分依據、明確各規格型號的區別。可采用對比表對不同規格型號的結構組成、性能指標加以描述。帶針的產品應同時說明縫針的規格型號信息、針線連接方式(如適用)。
4.包裝說明
提供與滅菌方法相適應的最初包裝的信息。初包裝內含液體成分的應說明液體的組成成分。
5.產品適用范圍和禁忌癥
(1)適用范圍:應當明確產品的適用范圍,包括預期的應用部位、縫合的組織類型、配合使用的器械(如適用)。
(2)禁忌癥:如適用,應當明確說明該產品禁忌應用的人群、疾病種類及縫合部位等。
6.參考的同類產品或前代產品:應當提供同類產品(國內外已上市)或前代產品(如有)的信息,闡述申請注冊產品的研發背景和目的。對于同類產品,應當說明選擇其作為研發參考的原因。
申請人應綜述該類產品國內外研究及臨床使用現狀及發展趨勢。列表比較說明本次申報產品與已上市同類及前代產品(如有)的相同點和不同點,比較的項目應包括產品名稱、原材料、涂層、結構、制式、性能指標、適用范圍、降解機理、生產工藝、滅菌方式、有效期、已上市國家等。
7.原材料控制
明確產品的起始物質,列明產品生產過程中由起始物質至終產品過程中所需全部材料的化學名稱、商品名/材料代號、CAS號、化學結構式/分子式、分子量/分子量范圍及分布、特性粘度、純度、使用量或組成比例、供應商名稱、符合的標準等基本信息,建議以列表的形式提供。
說明原材料的選擇依據,起始材料及來源,建議盡量選用已有相關人類臨床應用史的原材料。原材料應具有穩定的供貨渠道以保證產品質量,需提供原材料生產廠家的資質證明及外購協議。應明確所用原材料的質控標準及生產過程中的檢驗步驟,提交原材料符合相應標準的全性能驗證報告。若縫線單包裝中含液體成分,亦應提供液體的組成成分和質量控制文件。
對于首次應用于醫療器械的新材料,應提供該材料適合用于人體預期使用部位的相關研究資料。
對于動物源性原材料,如動物來源的膠原蛋白,還需要提交如下資料:
(1)動物的種屬、地理來源、年齡、取材部位(組織的類型和解剖來源)、動物及取材組織健康狀況的具體描述;
(2)對于常規定點飼養的動物種類,提供申請人與動物定點飼養單位簽訂的長期供貨協議及飼養單位的資質證明;如果涉及中間商,應提供所有中間商的有關供貨協議及資質證明;
(3)對于常規定點屠宰的動物種類,提供申請人(或動物源性材料供應商)與屠宰單位簽訂的合同及屠宰單位的資格證明;
(4)所取材動物的檢疫/防疫證明性資料,在我國一般包括動物檢疫合格證、動物防疫合格證、對動物進行防疫接種的獸醫衛生合格證等;
(5)申請人對保存每一批動物可追溯性文件(該文件中至少需包括:該產品所用動物的地理來源、取材部位、動物的可追溯性標識、動物飼養、檢疫、屠宰及加工方面的情況)的承諾。
注:這里提到的批是指在同一環境中飼養、檢疫、屠宰或加工的一組動物。
(二)研究資料
至少應包含如下內容:
1.產品性能研究
應當提供產品性能研究資料以及產品技術要求的研究和編制說明,包括有效性、安全性指標以及與質量控制相關的其他指標的確定依據、所采用的標準或方法、采用的原因及理論基礎等。
(1)物理性能研究
至少包括產品外觀、規格與直徑、抗張強度、長度、針線連接強度(如適用)、縫針性能(如適用,參考YY0043制定)等。
(2)化學性能研究
對于人工合成的可吸收縫線,應包括紅外及核磁鑒別、平均分子量、分子量分布(如適用)、單體殘留、催化劑殘留、溶劑殘留、含水量、重金屬含量、褪色試驗、環氧乙烷殘留量(如適用)、終產品中其他有害小分子物質的殘留量要求等。
對于動物源性材料制成的可吸收縫線,至少應包括材料定性要求、材料純度要求、重金屬殘留、可溶性鉻化合物試驗(鉻制縫線適用)、免疫原性或相關性能的控制指標(以證明產品的免疫原性可控制在可接受范圍)、終產品中有害物質的殘留量要求等。
(3)降解吸收性能研究
申請人應闡明產品的降解機理,建議提交支持降解機理的試驗資料或文獻資料。對于采用新材料制成的縫線,申請人應通過體內和體外試驗來證明可吸收縫線的降解吸收特性;對于采用成熟材料制成的縫線,申請人可通過體內或體外試驗來證明可吸收縫線的降解吸收特性,若僅進行體外試驗,還應提供體內-體外試驗相關性的支持性資料。申請人應提供降解周期、降解產物的研究資料,提供產品降解速率和產品主要性能(如抗張強度)隨著時間而變化的研究資料。降解特性說明中應包含圖表,以說明可吸收縫線的殘留抗張強度的持續時間具有臨床意義。具有臨床意義的時間長度取決于縫線的預期用途。建議申請人應指明吸收特性與預期用途(如組織縫合能力的保持時間)的一致性。
降解研究選擇的縫線規格應能覆蓋申請注冊的最大、最小及中等線徑的縫線規格進行研究。研究的縫線線徑規格之間的差異不得超過兩個規格,如要對規格從7至7-0的所有線徑規格縫線申請注冊,建議對7,4,1,2-0,5-0和7-0的縫線進行降解研究。
體外降解研究建議模擬體內條件,研究產品完全降解所需時間及所有的降解產物。建議結合產品特性及臨床應用建立合理的體外降解研究方法。建議參照已有的標準方法并與已上市的同類產品進行比較。體外降解研究建議考慮降解的中間產物與終產物的名稱、化學式、含量和對人體毒性的評價資料。
體內降解研究一般應是動物試驗研究,建議根據預期使用部位來研究產品的降解吸收特性,研究產品完全降解吸收所需時間及組織相容性等。
體內降解研究應說明選擇的動物種類及依據,建議選取多個中間時間點進行觀察,降解研究報告應說明所用材料、材料來源、研究設備、試驗方案、試驗步驟、支持文獻等。體內降解研究應根據縫線質量、尺寸、抗張強度等觀察指標對產品的降解程度進行評價。
申請人應提供產品在體內吸收代謝情況的文獻資料或研究資料。體內研究應對所申報產品及其降解產物在體內的吸收、分布、代謝及排泄途徑進行研究,可考慮但并不局限于以下內容:產品及其降解產物的吸收途徑、體內分布狀態、代謝途徑、代謝終產物對人體是否存在毒性作用、毒性作用的靶器官。
(4)無菌
(5)熱原
(6)特殊性能研究
若產品帶有抗菌涂層,申請人應對其抗菌性能開展研究。應進行體外試驗和體內試驗以對產品的抗菌作用機理、安全性、有效性進行初步評價。由于各個產品的材料、組成、作用機理不同,申請人應依據產品的特點進行試驗設計。
若產品帶有藥物涂層,應按照藥械組合產品增加對藥物涂層的相關要求。
對于申請人采用新材料制造的產品以及具有其他特殊性能的產品,企業應根據產品特點制定相應的性能要求,設計驗證該項特殊性能的試驗方法,闡明試驗方法的來源或提供方法學確認資料。
可參照的國家標準及行業標準舉例(未標明年代號表示應參照最新版本):
YY 1116《可吸收性外科縫線》
YY 0043《醫用縫合針》
YY/T 0661《外科植入物用聚(L-乳酸)樹脂的標準規范》
YY/T 0510《外科植入物用無定形聚丙交酯樹脂和丙交酯-乙交酯共聚樹脂》
YY/T 0640《無源外科植入物 通用要求》
GB/T 16886《醫療器械生物學評價》系列標準
GB/T 14233.1《醫用輸液、輸血、注射器具檢驗方法 第1部分:化學分析方法》
GB/T 14233.2《醫用輸液、輸血、注射器具檢驗方法 第2部分:生物學試驗方法》
《中華人民共和國藥典》
2.生物相容性評價研究
應按照GB/T 16886《醫療器械生物學評價》系列標準和YY 1116的規定進行可吸收縫線生物相容性研究。在試驗操作可行的前提下,部分生物學部分試驗項目可與上述產品性能研究項目一并進行。
3.生物安全性研究
對于動物源性材料的可吸收縫線,應按照動物源產品提交相關材料的生物安全性研究資料。應對生產過程中滅活和去除病毒和/或傳染性病原體工藝過程的描述及有效性驗證數據或相關資料,對清除(或降低)動物源性材料免疫原性工藝過程的描述、質量控制指標與驗證性實驗數據或相關資料。
4.滅菌工藝研究
(1)應明確滅菌工藝(方法和參數)及其選擇依據和無菌保證水平(SAL),并提供滅菌確認報告。可吸收縫線的無菌保證水平(SAL)應達到1×10-6。
(2)殘留毒性:若滅菌使用的方法容易出現殘留,如環氧乙烷滅菌,應當明確殘留物信息及采取的處理方法,并提供研究資料。
5.產品貨架有效期和包裝研究
(1)貨架有效期
貨架有效期包括產品有效期和包裝有效期。產品有效期驗證可采用實時老化或加速老化的研究。實時老化的研究是唯一能夠反映產品在規定儲存條件下實際穩定性要求的方法,應遵循極限試驗和過載試驗原則。加速老化研究試驗的具體要求可參考ASTM F1980(YY/T 0681.1)。
對于包裝的有效期驗證,建議提交在選擇恰當的材料和包裝結構合格后的最終成品包裝的初始完整性和維持完整性的檢測結果。在進行加速老化試驗研究時應注意:產品選擇的環境條件的老化機制應與與宣稱的運輸儲存條件真實下發生產品老化的機制相匹配一致。對于在加速老化研究中可能導致產品變性而不適于選擇加速老化試驗方法研究其包裝的有效期驗證,應以實時老化方法測定和驗證。
(2)包裝及包裝完整性:在宣稱的有效期內以及運輸儲存條件下,保持包裝完整性的依據。
產品包裝驗證可依據有關國內、國際標準進行(如GB/T 19633、ISO 11607、ASTM D-4169等),提交產品的包裝驗證報告。
6.其他資料
結合申報產品的特點,提交證明產品安全性、有效性的其他研究資料。
(三)生產制造信息
1.應當明確產品生產加工工藝,注明關鍵工藝和特殊工藝,并闡明其過程控制點及控制參數。對生產工藝的可控性、穩定性應進行確認。明確生產過程中各種加工助劑的使用情況及對雜質(如殘留單體、小分子殘留物等)的控制情況。
申請人需寫明主要反應過程、反應試劑、反應條件、催化劑、生成物、中間產物等,對每一步生產過程的非預期產物進行確認、分析,控制,提交非預期產物的質控標準、對人體安全性的評估資料等。
若生產過程涉及動物源性成分,應提供相應的病毒/病原體/免疫原性控制指標,控制指標的制定依據及方法、驗證等相關數據技術資料。
2.生產場地
有多個研制、生產場地,應當概述每個研制、生產場地的實際情況。
(四)產品的風險分析資料
按照YY 0316《醫療器械 風險管理對醫療器械的應用》標準的要求,對產品生命周期全過程實施風險管理。申請人在產品注冊上市前,應對風險管理過程進行評審。評審應至少確保:風險管理計劃已被適當地實施;綜合剩余風險是可接受的;已有適當方法獲得相關生產和生產后信息。評審結果應形成風險管理報告。風險管理資料應至少包括以下信息:
1.可能影響產品安全性的特征問題清單
應參考YY 0316附錄C的要求判定醫療器械與安全性有關特征的問題,但識別風險的來源并不局限于此。應對該類產品進行充分的風險識別,風險識別的信息來源需要具體列出,可包括但不局限于以下途徑:類似產品的投訴/抱怨數據、醫學文獻、試驗室檢測、動物試驗數據、產品標簽標識、專家觀點等。對于風險識別信息的來源企業應具體說明,并提交有關支持文件或文獻。
2.產品有關危害的清單
申請人應詳細列出與產品有關的已知和可預見危害的清單,以及對每個危害如何造成損害的分析(包括可預見的事件序列、危害處境和可能發生的損害)。
申請人應指出擬申報產品所特有的任何額外風險,說明風險分析的方法。已識別的風險應至少包括但不局限于以下方面:
(1)原材料的生物學和化學危害:
材料或材料來源變化;
原材料純度;
材料的生物相容性和可降解性能。
(2)生產加工過程可能產生的危害:
污染;
添加劑、助劑、輔劑的殘留;
病毒滅活;
免疫原性控制;
工藝用水;
生產環境潔凈度;
熱原;
內毒素。
(3)產品使用風險因素:
選擇與使用不當;
縫線斷裂;
感染;
傷口裂開;
異物反應引起的炎癥;
吸收緩慢或不吸收;
傷口愈合不良。
(4)滅菌過程可能產生的危害:
滅菌方式對產品不適宜,滅菌不完全等。
(5)不正確使用產生的危害:
未按照說明書中操作方法操作,使用過程中損傷 縫線等。
(6)產品包裝可能產生的危害:
包裝破損、標識不清等。
申請人應對所識別的風險提出具體的降低風險的措施。降低所申報產品的風險應依據YY 0316要求依次從設計、保護、說明書進行考慮。
申請人應在產品生命全周期中對風險進行管理控制,以使剩余風險在可接受范圍內。可通過產品設計控制、產品原材料選擇、產品技術性能指標的制定、動物試驗、臨床試驗、正確的標簽標識、滅菌等多項措施以降低風險至可接受水平,但不局限于上述內容。
(五)產品技術要求
申請人應結合產品的技術特征和臨床使用情況來確定產品安全有效、質量可控的技術要求與檢驗方法。產品技術要求中應明確規格型號及其劃分的說明、產品性能指標及試驗方法、產品描述一般信息(原材料、組成成分、結構、染色情況等)及產品包裝信息。產品技術要求中的內容引用國家標準、行業標準或中國藥典的,應保證其有效性,并注明相應標準的編號、年號及中國藥典的版本號。制定可吸收縫線技術要求的常用參考標準如下:
YY 1116《可吸收性外科縫線》
YY 0043《醫用縫合針》
GB/T 14233.1《醫用輸液、輸血、注射器具檢驗方法 第1部分:化學分析方法》
GB/T 14233.2《醫用輸液、輸血、注射器具檢驗方法 第2部分:生物學試驗方法》
《中華人民共和國藥典》
產品技術要求中的性能指標應不低于YY 1116《可吸收性外科縫線》中的相關要求,檢驗方法應采用行業標準中的方法,若采用其他方法則應選擇經驗證的方法并說明原因。除縫線材料及分類以外,技術要求中還應包括但不限于以下理化性能:外觀、規格與直徑、抗張強度、長度、可溶性鉻化合物試驗、重金屬、含水量要求、褪色試驗、環氧乙烷殘留量、降解性能、免疫原性或相關性能的控制指標(動物源性材料適用)。如縫線帶針,還應增加針線連接強度及縫合針的要求。縫線的生物性能應包括無菌和熱原。
對宣稱的所有其他技術參數和功能,均應在產品技術要求中予以規定。
若為動物源性原材料,應明確規定動物種屬、來源、年齡及取材部位。
產品技術要求的編制說明應說明產品性能指標及試驗方法制訂的依據。
(六)產品的注冊檢驗報告
申請人應提供具有醫療器械檢驗資質的醫療器械檢驗機構出具的注冊檢驗報告和預評價意見。此外,還應提供檢驗樣品規格型號的選擇依據。
所檢驗型號產品應當是本注冊單元內能夠代表申報的其他型號產品安全性和有效性的典型產品,若一個型號不能覆蓋,除選擇典型型號進行全性能檢驗外,還應選擇其他型號進行差異性檢驗。如:選擇最大、最小及中等尺寸的縫線規格進行物理性能的檢驗。檢驗的縫線尺寸之間的差異不得超過三個規格,如要對規格從7至7-0的所有尺寸縫線申請注冊,建議對7,4,1,2-0,5-0和7-0的縫線進行物理性能的檢驗。
不同色素和涂層的縫線應進行全性能檢驗。
(七)臨床評價
對于按照《醫療器械注冊管理辦法》規定需要進行臨床試驗的可吸收縫合線產品,臨床試驗應符合國家食品藥品監督管理總局頒布的《醫療器械臨床試驗質量管理規范》、《醫療器械臨床評價技術指導原則》及本指導原則制定臨床試驗方案并實施試驗。
臨床試驗時應注意如下幾方面:
1.臨床適應征的選擇
詳細說明試驗對象的選擇范圍、入選標準和排除標準,對照組的設置情況。
臨床試驗選擇的手術部位、組織類型應能覆蓋產品申報的臨床適用范圍。
2.評價指標
明確臨床性能評價指標,評價的指標應合理并便于臨床觀察,評價指標應包括有效性指標、安全性指標及術中操作性能評估指標。
以用于體表傷口為例:
(1)有效性評價指標為傷口愈合情況,包括以下內容:愈合進度、感染、水腫、紅斑、皮膚溫度、漿液瘤、縫線竇及疼痛評分(目測類比評分VAS:0分-10分)等。有效性評價指標的觀察終點為傷口愈合分級(甲級愈合、乙級愈合及丙級愈合)。
傷口愈合情況評估應分別于術后不同時間點進行,應同時記錄不良事件發生率以及可能影響傷口愈合的抗生素或其他藥物使用情況。
應對傷口可能造成不利影響的風險因素在試驗組和對照組中所占的比例是否相似進行分析。還應考慮兩組的靜脈抗生素治療情況。
(2)安全性評價指標:術后并發癥(切口感染、排異反應、瘢痕形成、切口裂開、切口疝)及不良反應。
(3)術中縫線操作性能指標(醫生盲態評估):
①穿越組織的難易程度;
②第一道結的繞線固定情況
③線結下系時是否順暢;
④線結的可靠性
⑤外科操作情況(包括外科手感)
⑥縫線記憶情況
從包裝中取出縫線及展開后,縫線應能保持相對穩定的線性結構。應該盡量沒有扭結、卷曲或其他有可能影響手術操作及使用的一些彎曲形態
⑦縫線的耐磨情況(抗撕解或抗拆開能力)。
3.研究設計和研究假設
建議申請人采用前瞻性、隨機對照設計,將擬申報器械與已獲準上市器械進行對比。對照器械應與擬申報器械采用類似的材料制成且具有相似的預期用途。
4.比較的類型
如優效性檢驗、非劣效性檢驗、等效性檢驗,申請人應說明選擇的依據。
5.樣本量確定依據
試驗例數應具有統計學意義,應足以確保所申報器械將能在臨床使用條件下充分發揮作用。
樣本量的大小應根據受試產品的具體特性、主要有效性(或安全性)評價指標及其估計值、顯著性水平、研究把握度以及臨床試驗比較的類型來確定。應在臨床試驗方案中明確給出具體的樣本量計算公式及其來源出處,說明計算過程中所采用的所有參數及其估計值。建議根據下列五個方面確定所需要的樣本量,即(1)擬采取的試驗設計類型(常分為單組設計、配對設計、成組設計、單因素多水平設計、交叉設計、析因設計、重復測量設計等);(2)擬采取的比較類型[常分為差異性檢驗(又分為單、雙側檢驗)、等效性檢驗、優效性檢驗和非劣效性檢驗];(3)參數選擇建議:Ⅰ類錯誤概率α值為雙側0.05(即單側0.025),Ⅱ類錯誤概率β通常不超過0.2(即把握度不小于80%);(4)主要評價指標的性質[通常分為定量的、定性的(又分為二值的和多值有序的)]和有關的基礎數據及有臨床意義的界值;(5)應考慮20%以內的脫落率。對于非劣效和等效性試驗,還應給出具有臨床意義的非劣效界值和/或等效性界值,若為優效性試驗,需要給出優效性界值。對各臨床試驗中心的入選受試者進行分組時,應盡可能基于重要的非試驗因素進行分層隨機化。
樣本量計算舉例(體表縫合為例)
將傷口達甲級愈合患者的比例作為主要評價指標,試驗采用隨機對照的非劣效設計,假設試驗組和對照組有效率(甲級愈合比例)均為98%,非劣效界值取5%,在統計學檢驗顯著性水平取單側0.025,把握度取80%時,每組至少需要入組124例患者,在此基礎上考慮10%的脫落率,最終每組的入選規模確定為138例。
所使用的樣本量計算公式為:
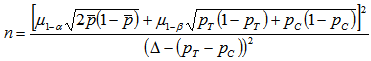
6.統計分析方法
應在方案中明確寫出將要采用的統計分析方法。所有統計分析均應在ITT(意向性治療)分析集進行,對于未能觀察到安全性或有效性終點的受試者,必須進行靈敏度分析,并按照失敗或者無效計算。
(1)描述性分析
計數資料采用頻數和百分比描述,計量資料采用均數、標準差、最大值、最小值、中位數、第25及第75分位數描述。
(2)基線人口統計學分析
基線統計除按上述描述性分析外,對計數資料組間比較采用卡方檢驗或Fisher精確概率法,正態分布的計量資料組間比較采用成組t檢驗,非正態分布的計量資料組間比較采用Wilcoxon秩和(Wilcoxon Rank Sum)檢驗。
(3)臨床終點選擇及分析
隨機對照設計的試驗,其主要終點有效率的組間比較,采用調整中心效應的CMH(Cochran Mantel-Haenszel)卡方檢驗,需給出試驗組與對照組有效率的差值及其95%可信區間,其余終點指標參照基線分析進行。
(4)安全性評價
為評估器械的安全性,建議申請人提交使用該器械時觀察到的所有不良事件和患者手術恢復期的全面評價,直到患者退出臨床研究。
實驗室指標:報告實驗室指標治療前正常、治療后異常的例數及所占比例,并進行組間比較。
不良事件:報告不良事件發生例數及所占比例,并進行組間比較。同時,詳細描述各組病例出現的全部不良事件的具體表現、程度及其與所使用的研究產品的關系。
7.試驗所用樣品的信息
應具體說明臨床試驗樣品的詳細信息:產品規格型號、批號、使用方法,對照品的詳細信息(生產廠家、產品材料、預期用途、使用方法、產品規格型號、批號、醫療器械注冊證號等)。
8.患者隨訪
建議對臨床試驗中納入的患者進行隨訪。隨訪應有客觀依據。
(八)產品說明書和標簽
產品說明書和標簽應符合《醫療器械說明書和標簽管理規定》(國家食品藥品監督管理總局令第6號)的要求,同時,還應滿足以下要求:
1.適應癥
應列出手術種類、身體部位、組織類型,并且在某些情況下,應說明縫線適用的預期患者人群。
2.說明書中應包含以下內容:
①說明材料組分或生物(物種和組織)來源;
②列出縫線的染料、涂層、所用的包裝液體;
③縫線的吸收方式和吸收速率;
④抗張強度隨著時間的變化情況;
⑤完全吸收所需的時間。
標簽內容應符合YY 1116的規定。
3.禁忌癥
應列出適用于可吸收縫線的禁忌癥。禁忌癥中應包含有:
證據證明不適用于縫線的手術類型、身體部位或患者人群。
4.警示信息
應列出適用于可吸收外科縫線的警告。警告中包括器械相關的嚴重不良反應或潛在的安全危害,并且還應包含可能的后果。舉例來講,“避免長期接觸尿液或膽汁”的警告,應包括后果情況,因此應聲明“長期接觸尿液或膽汁可能會導致結石形成”。
5.注意事項
應列出適用于縫線的注意事項。即將避免器械使用時的不良事件或潛在安全危害的措施告知用戶的聲明。比如,“用鑷子或持針器處理縫線時,應避免擠壓或卷曲縫線。擠壓或卷曲縫線可能會對縫線的抗張強度或吸收率造成不良影響”。(液體成分包裝的縫線在使用時應注明是否進行清洗及清洗步驟)與警告事項相同,注意事項中也應說明后果情況。
6.不良事件
應識別與縫線使用相關的不良事件。應單獨列出在所有縫線中觀察到的不良事件(僅在企業申報的縫線類型中觀察到的不良事件)。
7.應提交標簽、單包裝的印刷版示意圖。
可吸收性外科縫線:是可被人體組織吸收的外科縫線,可由健康哺乳動物的膠原或人工合成的聚合物等材料加工而成。
1.《醫療器械監督管理條例》(中華人民共和國國務院令第650號)
2.《醫療器械注冊管理辦法》(國家食品藥品監督管理總局令第4號)
3.《醫療器械說明書和標簽管理規定》(國家食品藥品監督管理總局令第6號)
4.《醫療器械臨床試驗質量管理規范》(國家食品藥品監督管理總局令第25號)
5.《關于公布醫療器械注冊申報資料要求和批準證明文件格式的公告》(國家食品藥品監督管理總局公告2014年第43號)
6.Class Ⅱ Special Controls Guidance Document: Surgical Suture;June 3, 2003;CDRH FDA.
國家食品藥品監督管理總局醫療器械技術審評中心

站點聲明
本網站所提供的信息僅供參考之用,并不代表本網贊同其觀點,也不代表本網對其真實性負責。圖片版權歸原作者所有,如有侵權請聯系我們,我們立刻刪除。如有關于作品內容、版權或其它問題請于作品發表后的30日內與本站聯系,本網將迅速給您回應并做相關處理。
鄭州思途醫療科技有限公司專注于醫療器械產品政策與法規規事務服務,提供產品注冊備案申報代理、臨床試驗、體系建立輔導、分類界定、申請創新辦理服務。

為深入貫徹落實中共中央辦公廳、國務院辦公廳印發的《關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》(廳字〔2017〕42號),按照國家藥品監督管理局《關于擴大醫療器械

為規范醫療器械注冊人跨區域委托生產的監督管理,推進長江三角洲區域醫療器械跨區域監管,根據《中共中央辦公廳國務院辦公廳關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》《

附件:血液透析用水處理設備注冊審查指導原則(2024年修訂版)(2024年第19號).doc血液透析用水處理設備注冊審查指導原則(2024年修訂版)本指導原則旨在指導注冊申請人對血液透析用水處理設備注冊申報資料的準備及撰寫,同時也為技術審評部門提供參考。本指導原則是對血液透析用水處理設備的一般要求,注冊申請人依據產品的具體特性確定其中內容是否適用。若不適用,要具體闡述理由及相應的科學依據,并依據產

本指導原則旨在幫助和指導注冊申請人對一次性使用腹部穿刺器注冊申報資料進行準備,以滿足技術審評的基本要求。同時有助于審評機構對該類產品進行科學規范的審評,提高審評工

國家藥監局關于發布免于臨床試驗的體外診斷試劑臨床評價技術指導原則的通告(2021年第74號)發布時間:2021-09-24為指導體外診斷試劑的臨床評價工作,根據

國家藥監局藥審中心關于發布《抗腫瘤藥物臨床試驗中SUSAR分析與處理技術指導原則》的通告(2024年第42號) 發布日期:20241010

國家市場監督管理總局令 第47號 《醫療器械注冊與備案管理辦法》已經2021年7月22日市場監管總局第11次局務會議通過,現予公布,自2021年10月1日起施行。 附件: 醫療器械注冊與備案管

國家藥監局器審中心關于發布影像型超聲診斷設備(第三類)注冊審查指導原則(2023年修訂版)的通告(2024年第29號)發布時間:2024-10-14為進一步規范

附件:醫用透明質酸鈉創面敷料注冊審查指導原則(2024年第21號).doc醫用透明質酸鈉創面敷料注冊審查指導原則本指導原則旨在指導注冊申請人準備及撰寫醫用透明質酸鈉創面敷料注冊申報資料,同時也為技術審評部門審查注冊申報資料提供參考。本指導原則是對醫用透明質酸鈉創面敷料產品的一般要求,注冊申請人應依據產品的具體特性確定其中內容是否適用,若不適用,需具體闡述理由及相應的科學依據,并依據產品的具體特性對

附件:重組膠原蛋白創面敷料注冊審查指導原則(2023年第16號).doc重組膠原蛋白創面敷料注冊審查指導原則本指導原則旨在指導注冊申請人準備及撰寫重組膠原蛋白創
行業資訊
知識分享
八年
醫療器械服務經驗
聯系思途,免費獲得專屬《落地解決方案》及報價
咨詢相關問題或咨詢報價,可以直接與我們聯系
思途CRO——醫療器械注冊臨床第三方平臺
