化妝品生產經營監督管理辦法(國家市場監督管理總局令第46號)
《化妝品生產經營監督管理辦法》已經2021年7月26日市場監管總局第12次局務會議通過,現予公布,自2022年1月1日起施行。
來源:醫療器械注冊代辦 發布日期:2014-07-30 閱讀量:次

國家食品藥品監督管理總局令
第 6 號
《醫療器械說明書和標簽管理規定》已于2014年6月27日經國家食品藥品監督管理總局局務會議審議通過,現予公布,自2014年10月1日起施行。
局長 張勇
2014年7月30日
第一條 為規范醫療器械說明書和標簽,保證醫療器械使用的安全,根據《醫療器械監督管理條例》,制定本規定。
第二條 凡在中華人民共和國境內銷售、使用的醫療器械,應當按照本規定要求附有說明書和標簽。
第三條 醫療器械說明書是指由醫療器械注冊人或者備案人制作,隨產品提供給用戶,涵蓋該產品安全有效的基本信息,用以指導正確安裝、調試、操作、使用、維護、保養的技術文件。
醫療器械標簽是指在醫療器械或者其包裝上附有的用于識別產品特征和標明安全警示等信息的文字說明及圖形、符號。
第四條 醫療器械說明書和標簽的內容應當科學、真實、完整、準確,并與產品特性相一致。
醫療器械說明書和標簽的內容應當與經注冊或者備案的相關內容一致。
醫療器械標簽的內容應當與說明書有關內容相符合。
第五條 醫療器械說明書和標簽對疾病名稱、專業名詞、診斷治療過程和結果的表述,應當采用統一發布或者規范的專用詞匯,度量衡單位應當符合相關標準的規定。
第六條 醫療器械說明書和標簽中使用的符號或者識別顏色應當符合相關標準的規定;無相關標準規定的,該符號及識別顏色應當在說明書中描述。
第七條 醫療器械最小銷售單元應當附有說明書。
醫療器械的使用者應當按照說明書使用醫療器械。
第八條 醫療器械的產品名稱應當使用通用名稱,通用名稱應當符合藥監總局制定的醫療器械命名規則。第二類、第三類醫療器械的產品名稱應當與醫療器械注冊證中的產品名稱一致。
產品名稱應當清晰地標明在說明書和標簽的顯著位置。
第九條 醫療器械說明書和標簽文字內容應當使用中文,中文的使用應當符合通用的語言文字規范。醫療器械說明書和標簽可以附加其他文種,但應當以中文表述為準。
醫療器械說明書和標簽中的文字、符號、表格、數字、圖形等應當準確、清晰、規范。
第十條 醫療器械說明書一般應當包括以下內容:
(一)產品名稱、型號、規格;
(二)注冊人或者備案人的名稱、住所、聯系方式及售后服務單位,進口醫療器械還應當載明代理人的名稱、住所及聯系方式;
(三)生產企業的名稱、住所、生產地址、聯系方式及生產許可證編號或者生產備案憑證編號,委托生產的還應當標注受托企業的名稱、住所、生產地址、生產許可證編號或者生產備案憑證編號;
(四)醫療器械注冊證編號或者備案憑證編號;
(五)產品技術要求的編號;
(六)產品性能、主要結構組成或者成分、適用范圍;
(七)禁忌癥、注意事項、警示以及提示的內容;
(八)安裝和使用說明或者圖示,由消費者個人自行使用的醫療器械還應當具有安全使用的特別說明;
(九)產品維護和保養方法,特殊儲存、運輸條件、方法;
(十)生產日期,使用期限或者失效日期;
(十一)配件清單,包括配件、附屬品、損耗品更換周期以及更換方法的說明等;
(十二)醫療器械標簽所用的圖形、符號、縮寫等內容的解釋;
(十三)說明書的編制或者修訂日期;
(十四)其他應當標注的內容。
第十一條 醫療器械說明書中有關注意事項、警示以及提示性內容主要包括:
(一)產品使用的對象;
(二)潛在的安全危害及使用限制;
(三)產品在正確使用過程中出現意外時,對操作者、使用者的保護措施以及應當采取的應急和糾正措施;
(四)必要的監測、評估、控制手段;
(五)一次性使用產品應當注明“一次性使用”字樣或者符號,已滅菌產品應當注明滅菌方式以及滅菌包裝損壞后的處理方法,使用前需要消毒或者滅菌的應當說明消毒或者滅菌的方法;
(六)產品需要同其他醫療器械一起安裝或者聯合使用時,應當注明聯合使用器械的要求、使用方法、注意事項;
(七)在使用過程中,與其他產品可能產生的相互干擾及其可能出現的危害;
(八)產品使用中可能帶來的不良事件或者產品成分中含有的可能引起副作用的成分或者輔料;
(九)醫療器械廢棄處理時應當注意的事項,產品使用后需要處理的,應當注明相應的處理方法;
(十)根據產品特性,應當提示操作者、使用者注意的其他事項。
第十二條 重復使用的醫療器械應當在說明書中明確重復使用的處理過程,包括清潔、消毒、包裝及滅菌的方法和重復使用的次數或者其他限制。
第十三條 醫療器械標簽一般應當包括以下內容:
(一)產品名稱、型號、規格;
(二)注冊人或者備案人的名稱、住所、聯系方式,進口醫療器械還應當載明代理人的名稱、住所及聯系方式;
(三)醫療器械注冊證編號或者備案憑證編號;
(四)生產企業的名稱、住所、生產地址、聯系方式及生產許可證編號或者生產備案憑證編號,委托生產的還應當標注受托企業的名稱、住所、生產地址、生產許可證編號或者生產備案憑證編號;
(五)生產日期,使用期限或者失效日期;
(六)電源連接條件、輸入功率;
(七)根據產品特性應當標注的圖形、符號以及其他相關內容;
(八)必要的警示、注意事項;
(九)特殊儲存、操作條件或者說明;
(十)使用中對環境有破壞或者負面影響的醫療器械,其標簽應當包含警示標志或者中文警示說明;
(十一)帶放射或者輻射的醫療器械,其標簽應當包含警示標志或者中文警示說明。
醫療器械標簽因位置或者大小受限而無法全部標明上述內容的,至少應當標注產品名稱、型號、規格、生產日期和使用期限或者失效日期,并在標簽中明確“其他內容詳見說明書”。
第十四條 醫療器械說明書和標簽不得有下列內容:
(一)含有“療效最佳”、“保證治愈”、“包治”、“根治”、“即刻見效”、“完全無毒副作用”等表示功效的斷言或者保證的;
(二)含有“最高技術”、“最科學”、“最先進”、“最佳”等絕對化語言和表示的;
(三)說明治愈率或者有效率的;
(四)與其他企業產品的功效和安全性相比較的;
(五)含有“保險公司保險”、“無效退款”等承諾性語言的;
(六)利用任何單位或者個人的名義、形象作證明或者推薦的;
(七)含有誤導性說明,使人感到已經患某種疾病,或者使人誤解不使用該醫療器械會患某種疾病或者加重病情的表述,以及其他虛假、夸大、誤導性的內容;
(八)法律、法規規定禁止的其他內容。
第十五條 醫療器械說明書應當由注冊申請人或者備案人在醫療器械注冊或者備案時,提交食品藥品監督管理部門審查或者備案,提交的說明書內容應當與其他注冊或者備案資料相符合。
第十六條 經食品藥品監督管理部門注冊審查的醫療器械說明書的內容不得擅自更改。
已注冊的醫療器械發生注冊變更的,申請人應當在取得變更文件后,依據變更文件自行修改說明書和標簽。
說明書的其他內容發生變化的,應當向醫療器械注冊的審批部門書面告知,并提交說明書更改情況對比說明等相關文件。審批部門自收到書面告知之日起20個工作日內未發出不予同意通知件的,說明書更改生效。
第十七條 已備案的醫療器械,備案信息表中登載內容、備案產品技術要求以及說明書其他內容發生變化的,備案人自行修改說明書和標簽的相關內容。
第十八條 說明書和標簽不符合本規定要求的,由縣級以上藥監管理部門按照《醫療器械監督管理條例》第六十七條的規定予以處罰。
第十九條 本規定自2014年10月1日起施行。2004年7月8日公布的《醫療器械說明書、標簽和包裝標識管理規定》(原藥監總局令第10號)同時廢止。

站點聲明
本網站所提供的信息僅供參考之用,并不代表本網贊同其觀點,也不代表本網對其真實性負責。圖片版權歸原作者所有,如有侵權請聯系我們,我們立刻刪除。如有關于作品內容、版權或其它問題請于作品發表后的30日內與本站聯系,本網將迅速給您回應并做相關處理。
鄭州思途醫療科技有限公司專注于醫療器械產品政策與法規規事務服務,提供產品注冊備案申報代理、臨床試驗、體系建立輔導、分類界定、申請創新辦理服務。

《化妝品生產經營監督管理辦法》已經2021年7月26日市場監管總局第12次局務會議通過,現予公布,自2022年1月1日起施行。
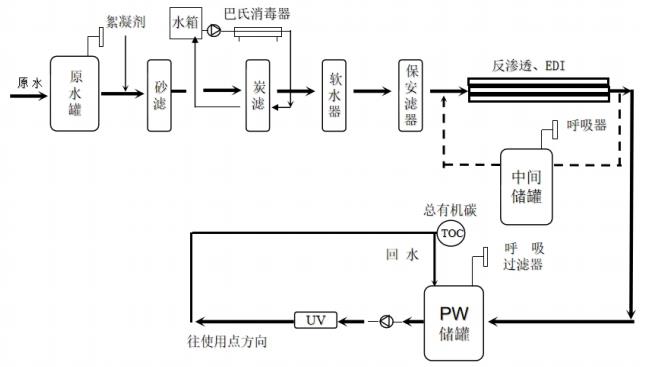
為規范醫療器械現場檢查,提升檢查員現場檢查能力,指導檢查員對醫療器械生產企業工藝用水控制情況的檢查,提高企業工藝用水質量安全保證水平,依據《醫療器械監督管理條例》
《海南博鰲樂城國際醫療旅游先行區臨床急需進口藥品帶離先行區使用管理暫行辦法》已經3月24日海南博鰲樂城國際醫療旅游先行區領導小組會議審議通過,現印發給你們,請遵照執行

為深入貫徹落實中共中央辦公廳、國務院辦公廳印發的《關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》(廳字〔2017〕42號),按照國家藥品監督管理局《關于擴大醫療器械
《化妝品監督管理條例》已經2020年1月3日國務院第77次常務會議通過,現予公布,自2021年1月1日起施行。

為規范醫療器械注冊人跨區域委托生產的監督管理,推進長江三角洲區域醫療器械跨區域監管,根據《中共中央辦公廳國務院辦公廳關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》《
《海南博鰲樂城國際醫療旅游先行區醫療機構制劑調劑使用管理暫行辦法》已經3月24日海南博鰲樂城國際醫療旅游先行區領導小組會議審議通過,現印發給你們,請遵照執行。

關于發布醫療器械質量管理體系年度自查報告編寫指南的通告(2022年第13號)發布時間:2022-03-24為加強醫療器械生產監管,保障醫療器械安全有效,根據《醫

國家藥監局關于發布免于進行臨床評價醫療器械目錄的通告(2025年第19號)發布時間:2025-05-13為做好醫療器械注冊管理工作,根據《醫療器械注冊與備案管理

《醫療器械監督管理條例》已經2020年12月21日國務院第119次常務會議修訂通過,現予公布,自2021年6月1日起施行。
行業資訊
知識分享
八年
醫療器械服務經驗
聯系思途,免費獲得專屬《落地解決方案》及報價
咨詢相關問題或咨詢報價,可以直接與我們聯系
思途CRO——醫療器械注冊臨床第三方平臺
