有源醫(yī)療器械加速老化試驗(yàn)效期驗(yàn)證及使用期限驗(yàn)證流程
為了確保醫(yī)療器械在生命周期內(nèi)的安全及有效性,注冊人應(yīng)在設(shè)計(jì)開發(fā)中對其使用期限予以驗(yàn)證。使用期限的驗(yàn)證是醫(yī)療器械可靠性研究的重要組成部分,制定并驗(yàn)證合理的使用期限有


注冊備案 · 臨床試驗(yàn) · 體系建立輔導(dǎo) · 分類界定 · 申請創(chuàng)新
來源:醫(yī)療器械注冊代辦 發(fā)布日期:2023-10-10 閱讀量:次
?
——兼評《醫(yī)療器械監(jiān)督管理?xiàng)l例(修訂草案)》通過
2020年12月21日,國務(wù)院常務(wù)會議審議通過了《醫(yī)療器械監(jiān)督管理?xiàng)l例(修訂草案)》(以下簡稱《修訂草案》),意味著醫(yī)療器械行業(yè)母法第三次大修改即將接近尾聲。這次修改是在醫(yī)療器械注冊人制度試點(diǎn)的大背景下進(jìn)行的,引起了行業(yè)產(chǎn)業(yè)的高度關(guān)注。

自2000年《醫(yī)療器械監(jiān)督管理?xiàng)l例》實(shí)施以來,在全國人大沒有出臺《醫(yī)療器械管理法》的情形下,該《條例》實(shí)際上成為了醫(yī)療器械行業(yè)的根本大法。以《條例》為核心,相關(guān)配套規(guī)章為輔助形成了貫徹醫(yī)療器械產(chǎn)品全生命周期的法規(guī)體系。但一直以來,醫(yī)療器械法規(guī)體系內(nèi)容分散,基本分段而立,并沒有找到“主心骨”將這些分布于不同環(huán)節(jié)的制度整合成基本制度。本次《條例》修訂中,將醫(yī)療器械注冊人、備案人等主體的權(quán)利義務(wù)貫穿于產(chǎn)品全生命周期的各個(gè)環(huán)節(jié),使醫(yī)療器械注冊人制度作為行業(yè)的基本制度得以鞏固。自此,醫(yī)療器械行業(yè)大法將有了自己的“主心骨”,為后續(xù)《條例》上升為《醫(yī)療器械管理法》奠定必要的法律基礎(chǔ)。
《條例》本次修訂,仍然沿襲“全程嚴(yán)格監(jiān)管”的主軸行文布局,絲毫沒有因?yàn)樾袠I(yè)欣欣向榮而有監(jiān)管力度的松懈。這次修訂,進(jìn)一步細(xì)化了處罰情形,并加大了嚴(yán)重違法情形的處罰力度。從處罰到人到行業(yè)禁入,從嚴(yán)格行政責(zé)任到追究刑事責(zé)任,凸顯的是政府從嚴(yán)監(jiān)管醫(yī)療器械行業(yè)的決心和魄力。從《條例》修訂中,我們看到的是,責(zé)任高企、紅線高舉,在進(jìn)一步總結(jié)監(jiān)管科學(xué)成果創(chuàng)新監(jiān)管制度的同時(shí),對醫(yī)療器械違法行為零容忍、嚴(yán)處置的態(tài)勢不會改變。
在這樣的背景下,合規(guī)自然就成為最好的競爭力。醫(yī)療器械行業(yè)企業(yè)需要及時(shí)、主動、全面、準(zhǔn)確地履行自己的法規(guī)義務(wù),不能有偷工減料之念、不得有投機(jī)取巧之心,否則就會被法規(guī)繪制的紅線束縛而動彈不得。《條例》對于無證生產(chǎn)經(jīng)營醫(yī)療器械或生產(chǎn)經(jīng)營無證醫(yī)療器械的行為,最高可處貨值金額30倍的罰款。這樣的罰款力度史無前例、力度空前,足以讓違法者傾家蕩產(chǎn)。因此,合規(guī)才是企業(yè)行穩(wěn)致遠(yuǎn)的法寶,合規(guī)才是企業(yè)保駕護(hù)航的利器。
醫(yī)療器械技術(shù)復(fù)雜、學(xué)科交叉性強(qiáng),既事關(guān)人民生命安全和身體健康,又關(guān)系國家經(jīng)濟(jì)發(fā)展和社會穩(wěn)定,因此醫(yī)療器械行業(yè)就是名副其實(shí)的“強(qiáng)監(jiān)管、嚴(yán)管理”的行業(yè)。監(jiān)管部門三令五申,促質(zhì)量高線,保安全底線。同時(shí)又苦口婆心,出指導(dǎo)文件,推制度革新。只有明白監(jiān)管部門的良苦用心,才能深刻領(lǐng)會本次《條例》修訂的精髓。
守法的前提是學(xué)法,全面、正確、系統(tǒng)地把握法規(guī)的內(nèi)容是將守法轉(zhuǎn)化為最優(yōu)生產(chǎn)力的必要條件。本次《條例》修訂設(shè)立了附條件醫(yī)療器械審批、醫(yī)療器械臨床拓展性應(yīng)用等多個(gè)新制度,利用好這些制度就能轉(zhuǎn)化為我們行業(yè)企業(yè)的生產(chǎn)力。在注冊人制度試點(diǎn)經(jīng)驗(yàn)的積累下,注冊人制度全面正式實(shí)施將給產(chǎn)業(yè)創(chuàng)新帶來推進(jìn)作用。變道超車、占領(lǐng)競爭制高點(diǎn)除了需要綜合運(yùn)用資本、技術(shù)、人才等多種要素,但在從嚴(yán)監(jiān)管的環(huán)境下,守法一旦成為短板,勢必釀成前功盡棄之苦果。因此,在依法治國和從嚴(yán)監(jiān)管的趨勢下,守法就是最優(yōu)的生產(chǎn)力。
《條例》三度修訂,數(shù)易其稿,是醫(yī)療器械法規(guī)集大成者!此次修訂發(fā)出的合規(guī)信號,不應(yīng)被行業(yè)企業(yè)所忽略。《條例》的修訂,還將帶動《醫(yī)療器械注冊管理辦法》《醫(yī)療器械生產(chǎn)監(jiān)督管理辦法》《醫(yī)療器械經(jīng)營監(jiān)督管理辦法》《醫(yī)療器械使用質(zhì)量監(jiān)督管理辦法》等配套部門規(guī)章的修訂。監(jiān)管規(guī)則的重塑會引發(fā)行業(yè)格局的重新洗牌,醫(yī)療器械行業(yè)的健康發(fā)展,有賴于一大批奉合規(guī)為圭臬、視守法為生命的行業(yè)人士的努力。
上海健康醫(yī)學(xué)院、東南大學(xué)蘇州醫(yī)療器械研究院、東勱醫(yī)療科技三方共同發(fā)起成立的“醫(yī)療器械合規(guī)研究中心”將以合規(guī)研究為己任,為行業(yè)企業(yè)輸出公益性的醫(yī)療器械合規(guī)研究成果。我們相信,在新修訂《條例》的引領(lǐng)下,未來將是唯合規(guī)者贏、唯守法者勝的時(shí)代。
作者:蔣海洪

站點(diǎn)聲明
本網(wǎng)站所提供的信息僅供參考之用,并不代表本網(wǎng)贊同其觀點(diǎn),也不代表本網(wǎng)對其真實(shí)性負(fù)責(zé)。圖片版權(quán)歸原作者所有,如有侵權(quán)請聯(lián)系我們,我們立刻刪除。如有關(guān)于作品內(nèi)容、版權(quán)或其它問題請于作品發(fā)表后的30日內(nèi)與本站聯(lián)系,本網(wǎng)將迅速給您回應(yīng)并做相關(guān)處理。
鄭州思途醫(yī)療科技有限公司專注于醫(yī)療器械產(chǎn)品政策與法規(guī)規(guī)事務(wù)服務(wù),提供產(chǎn)品注冊備案申報(bào)代理、臨床試驗(yàn)、體系建立輔導(dǎo)、分類界定、申請創(chuàng)新辦理服務(wù)。
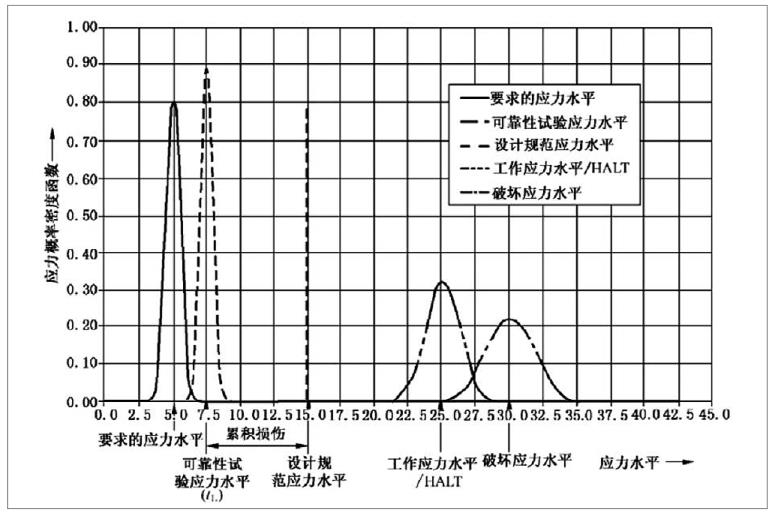
為了確保醫(yī)療器械在生命周期內(nèi)的安全及有效性,注冊人應(yīng)在設(shè)計(jì)開發(fā)中對其使用期限予以驗(yàn)證。使用期限的驗(yàn)證是醫(yī)療器械可靠性研究的重要組成部分,制定并驗(yàn)證合理的使用期限有

國家市場監(jiān)管總局于官網(wǎng)公布《藥品注冊管理辦法》(以下簡稱“辦法”)已于2020年7月1日起正式施行。國家藥監(jiān)局從《辦法》修訂的背景、思路、引入了哪些新理念和制度、有哪些鼓
中國是世界上最有潛力的醫(yī)療器械市場及最大市場之一,許多醫(yī)療器械進(jìn)出口貿(mào)易商或國外有實(shí)力的企業(yè)希望能夠按照中國藥監(jiān)局醫(yī)療器械注冊監(jiān)管要求獲得中國市場的上市準(zhǔn)入。考慮

醫(yī)療器械注冊費(fèi)是行政性收費(fèi),按照注冊單元收取,部分省份不收取醫(yī)療器械注冊費(fèi)用,絕大部分省份還是收取的。本篇文章統(tǒng)計(jì)了截止到2022年1月5日各地醫(yī)療器械注冊收費(fèi)標(biāo)準(zhǔn)。

中國能排進(jìn)世界十大醫(yī)療器械制造強(qiáng)國嗎?暫時(shí)還不能,因?yàn)榕胚M(jìn)前十的國家都有許多知名械企和世界級醫(yī)療器械巨頭;而中國比較出名的可能只有邁瑞了,其他械企仍需努力了。下面

2020年3月17日國家藥監(jiān)局發(fā)布了關(guān)于醫(yī)療器械主文檔登記事項(xiàng)的公告(2021年第36號),之前給大家介紹過醫(yī)療器械主文檔的主要內(nèi)容、適用的產(chǎn)品注冊類型等信息。今天我們再來向大家介

本文介紹了歐盟醫(yī)療器械新法規(guī)MDR相比于將替代的MDD法規(guī)的幾點(diǎn)新增要求。建議收藏學(xué)習(xí)。明年5月份起,Medical Devices Regulation(MDR)(2017/745/ EU)將替代原本的Medical Devices Directive (93

潤滑劑類產(chǎn)品在美國根據(jù)產(chǎn)品預(yù)期用途的不同主要分為人體潤滑劑和患者潤滑劑:其中,人體潤滑劑主要成分為水、丙二醇、羥乙基纖維素、苯甲酸、卡波姆、氫氧化鈉等,作用于生殖

2021年2月5日,湖南省藥監(jiān)局分別與湖南省計(jì)量檢測研究院、湖南新領(lǐng)航檢測技術(shù)有限公司、湖南普瑞瑪藥物研究中心有限公司、深圳華通威國際檢驗(yàn)有限公司、南德認(rèn)證檢測(中國)有限公

為規(guī)范醫(yī)療器械(含體外診斷試劑)注冊管理,根據(jù)國家藥監(jiān)局《關(guān)于公布醫(yī)療器械注冊申報(bào)資料要求和批準(zhǔn)證明文件格式的公告》(2021年第121號)、《關(guān)于公布體外診斷試劑注冊申報(bào)
行業(yè)資訊
知識分享
法規(guī)文件
?
?
?
?
?
?
八年
醫(yī)療器械服務(wù)經(jīng)驗(yàn)
聯(lián)系思途,免費(fèi)獲得專屬《落地解決方案》及報(bào)價(jià)
咨詢相關(guān)問題或咨詢報(bào)價(jià),可以直接與我們聯(lián)系
思途CRO——醫(yī)療器械注冊臨床第三方平臺
