有源醫(yī)療器械加速老化試驗效期驗證及使用期限驗證流程
為了確保醫(yī)療器械在生命周期內(nèi)的安全及有效性,注冊人應在設計開發(fā)中對其使用期限予以驗證。使用期限的驗證是醫(yī)療器械可靠性研究的重要組成部分,制定并驗證合理的使用期限有


注冊備案 · 臨床試驗 · 體系建立輔導 · 分類界定 · 申請創(chuàng)新
來源:醫(yī)療器械注冊代辦 發(fā)布日期:2023-10-10 閱讀量:次
?
近日,湖南省藥品監(jiān)督管理局發(fā)布公告,決定對第二、三類醫(yī)療器械生產(chǎn)許可行政審批事項實行全程無紙化網(wǎng)上辦理,即實現(xiàn)第二、三類醫(yī)療器械生產(chǎn)許可“網(wǎng)上申報、網(wǎng)上受理、網(wǎng)上審批”,自2021年4月19日起正式實施。
醫(yī)療器械生產(chǎn)企業(yè)申報生產(chǎn)許可事項和提交生產(chǎn)許可現(xiàn)場檢查缺陷項目整改資料時,可通過湖南政務服務網(wǎng)或者湖南省藥品監(jiān)督管理局網(wǎng)站登錄行政審批系統(tǒng),網(wǎng)上提交申請表格、申請資料和整改資料。提交資料后,可以登錄審批系統(tǒng)查詢辦件狀態(tài)和補正通知,已經(jīng)受理的許可申報事項,可以在湖南省藥品監(jiān)管局網(wǎng)站網(wǎng)上辦事欄目和湖南政務服務網(wǎng)站“我要查”欄目通過辦件編碼查詢辦理進度。行政審批決定后,政務窗口制作《醫(yī)療器械生產(chǎn)許可證》,并按照企業(yè)提交申報資料時選擇的方式(郵寄送達或窗口現(xiàn)場自取)獲取證書。
近年來,省藥品監(jiān)督管理局堅持以 “保安全、促發(fā)展、提幸福”為基本工作目標,積極探索改革審批管理方式,全面落實省政府“互聯(lián)網(wǎng)+政務服務”“三集中三到位”“一件事一次辦”,提高行政審批服務效能,全面落實企業(yè)主體責任,助力全省生物醫(yī)藥產(chǎn)業(yè)高質量發(fā)展。實施第二、三類醫(yī)療器械生產(chǎn)許可全程無紙化網(wǎng)上辦理,是省藥品監(jiān)督管理局推進“放管服”改革,深化醫(yī)療器械審評審批制度改革系列舉措之一。
以下為公告原文:

發(fā)布時間:2021年03月31日 11:21信息來源:湖南省藥品監(jiān)督管理局
為持續(xù)深化“放管服”改革,全面落實省政府“互聯(lián)網(wǎng)+政務服務”“三集中三到位”“一件事一次辦”工作部署,全面提升政務服務效能,我局決定對第二、三類醫(yī)療器械生產(chǎn)許可行政審批事項實行全程無紙化網(wǎng)上辦理(以下簡稱網(wǎng)辦),即實現(xiàn)第二、三類醫(yī)療器械生產(chǎn)許可“網(wǎng)上申報、網(wǎng)上受理、網(wǎng)上審批”,現(xiàn)將有關事宜公告如下:
2021年4月19日起,省內(nèi)第二、三類醫(yī)療器械生產(chǎn)許可證核發(fā)、生產(chǎn)許可證變更許可、生產(chǎn)許可證延續(xù),全部實行網(wǎng)上電子提交和電子審批。
2021年4月19日前受理的,按原有流程辦理。
醫(yī)療器械生產(chǎn)企業(yè)(以下簡稱申請人)申報生產(chǎn)許可事項和提交生產(chǎn)許可現(xiàn)場檢查缺陷項目整改資料時,應當通過湖南政務服務網(wǎng)或者湖南省藥品監(jiān)督管理局網(wǎng)站登錄行政審批系統(tǒng),網(wǎng)上提交申請表格、申請資料和整改資料(申請資料目錄、相關表格及示范文本詳見湖南政務服務網(wǎng)或者省藥品監(jiān)管局網(wǎng)站)。網(wǎng)上提交資料時,應當上傳加蓋申請人公章原件的PDF掃描文檔。申請人對網(wǎng)上申請和提交資料相關信息的真實性、準確性、完整性、有效性負責。
申請人提交申報資料后,省局政務窗口對資料進行形式審查,符合法定條件和要求的,依法予以受理;經(jīng)審查依法需要補正資料的,通過審批系統(tǒng)一次性告知需要補正資料。查驗機構對申報資料審核過程中,確需申請人補充完善資料的,由申請人在整改環(huán)節(jié)一并在網(wǎng)上提交。
申請人提交資料后,可以登錄審批系統(tǒng)查詢辦件狀態(tài)和補正通知,已經(jīng)受理的許可申報事項,申請人可以在湖南省藥品監(jiān)管局網(wǎng)站網(wǎng)上辦事欄目和湖南政務服務網(wǎng)站“我要查”欄目通過辦件編碼查詢辦理進度。
行政審批決定后,政務窗口制作《醫(yī)療器械生產(chǎn)許可證》,并按照申請人提交申報資料時選擇的方式(郵寄送達或窗口現(xiàn)場自取)獲取證書。申請人在領取證書前,須將原《醫(yī)療器械生產(chǎn)許可證》收回或寄回。
(一)生產(chǎn)許可辦理結果將以短信方式提醒申請人,申請人應確保聯(lián)系人手機號碼準確、有效,可接收短信。
(二)申請人在辦理中遇到網(wǎng)上申報、受理、資料電子轉化等方面問題的,可與省局相關業(yè)務受理部門聯(lián)系。
醫(yī)療器械監(jiān)管處電話:0731-88633320
政務大廳窗口電話:0731-82213698
技術咨詢電話:0731-88633388、88633389
政務窗口地址:長沙市天心區(qū)銀杏路6號,省政務服務中心。
附件:Ⅱ、Ⅲ類醫(yī)療器械生產(chǎn)許可流程及材料清單.doc
湖南省藥品監(jiān)督管理局
2021年3月31日


站點聲明
本網(wǎng)站所提供的信息僅供參考之用,并不代表本網(wǎng)贊同其觀點,也不代表本網(wǎng)對其真實性負責。圖片版權歸原作者所有,如有侵權請聯(lián)系我們,我們立刻刪除。如有關于作品內(nèi)容、版權或其它問題請于作品發(fā)表后的30日內(nèi)與本站聯(lián)系,本網(wǎng)將迅速給您回應并做相關處理。
鄭州思途醫(yī)療科技有限公司專注于醫(yī)療器械產(chǎn)品政策與法規(guī)規(guī)事務服務,提供產(chǎn)品注冊備案申報代理、臨床試驗、體系建立輔導、分類界定、申請創(chuàng)新辦理服務。
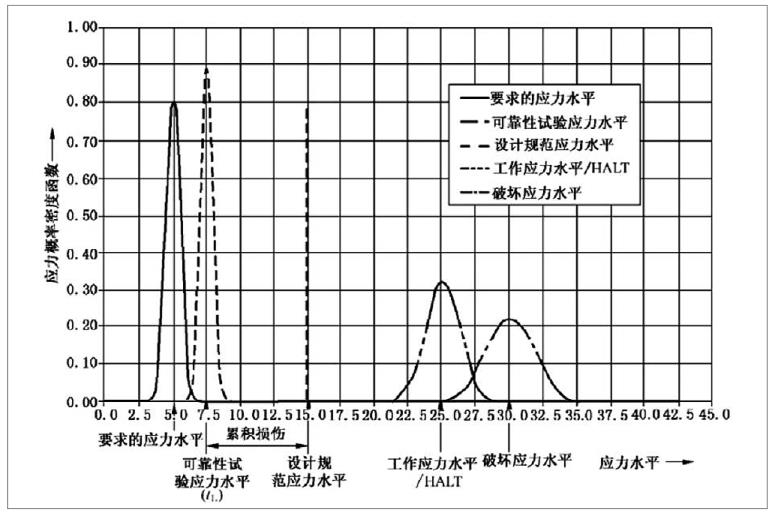
為了確保醫(yī)療器械在生命周期內(nèi)的安全及有效性,注冊人應在設計開發(fā)中對其使用期限予以驗證。使用期限的驗證是醫(yī)療器械可靠性研究的重要組成部分,制定并驗證合理的使用期限有
中國是世界上最有潛力的醫(yī)療器械市場及最大市場之一,許多醫(yī)療器械進出口貿(mào)易商或國外有實力的企業(yè)希望能夠按照中國藥監(jiān)局醫(yī)療器械注冊監(jiān)管要求獲得中國市場的上市準入。考慮

醫(yī)療器械注冊費是行政性收費,按照注冊單元收取,部分省份不收取醫(yī)療器械注冊費用,絕大部分省份還是收取的。本篇文章統(tǒng)計了截止到2022年1月5日各地醫(yī)療器械注冊收費標準。

中國能排進世界十大醫(yī)療器械制造強國嗎?暫時還不能,因為排進前十的國家都有許多知名械企和世界級醫(yī)療器械巨頭;而中國比較出名的可能只有邁瑞了,其他械企仍需努力了。下面

2020年3月17日國家藥監(jiān)局發(fā)布了關于醫(yī)療器械主文檔登記事項的公告(2021年第36號),之前給大家介紹過醫(yī)療器械主文檔的主要內(nèi)容、適用的產(chǎn)品注冊類型等信息。今天我們再來向大家介

本文介紹了歐盟醫(yī)療器械新法規(guī)MDR相比于將替代的MDD法規(guī)的幾點新增要求。建議收藏學習。明年5月份起,Medical Devices Regulation(MDR)(2017/745/ EU)將替代原本的Medical Devices Directive (93

潤滑劑類產(chǎn)品在美國根據(jù)產(chǎn)品預期用途的不同主要分為人體潤滑劑和患者潤滑劑:其中,人體潤滑劑主要成分為水、丙二醇、羥乙基纖維素、苯甲酸、卡波姆、氫氧化鈉等,作用于生殖

2021年2月5日,湖南省藥監(jiān)局分別與湖南省計量檢測研究院、湖南新領航檢測技術有限公司、湖南普瑞瑪藥物研究中心有限公司、深圳華通威國際檢驗有限公司、南德認證檢測(中國)有限公

為規(guī)范醫(yī)療器械(含體外診斷試劑)注冊管理,根據(jù)國家藥監(jiān)局《關于公布醫(yī)療器械注冊申報資料要求和批準證明文件格式的公告》(2021年第121號)、《關于公布體外診斷試劑注冊申報

浙江省藥品監(jiān)督管理局發(fā)布公告,進一步放開第三方醫(yī)療器械檢驗至6家。"
行業(yè)資訊
知識分享
八年
醫(yī)療器械服務經(jīng)驗
聯(lián)系思途,免費獲得專屬《落地解決方案》及報價
咨詢相關問題或咨詢報價,可以直接與我們聯(lián)系
思途CRO——醫(yī)療器械注冊臨床第三方平臺
